А́томний ра́діус — величина, що визначається розмірами електронної оболонки атома і дорівнює середній відстані між ядром атома та найвіддаленішою орбітальною електронною оболонкою атома. Атомний радіус вимірюється в пікометрах або ангстремах.
Радіуси атомів в кожному періоді зменшуються зліва на право, а в групі збільшуються зверху до низу. Хімічні властивості атомів обумовлені їх здатністю віддавати електрони або їх приймати. Чим більше радіус атома, тим слабше утримуються його зовнішні електрони.
Лютецій
| Лютецій (Lu) | |
|---|---|
| Радіус атома | 175 пм |
| Енергія іонізації (перший електрон) | 513,0(5,32) кДж/моль (еВ) |
| Електронна конфігурація | [Xe] 4f14 5d1 6s2 |
| Хімічні властивості |
Періодичність властивостей елементів Атомний радіус — збільшується зверху до низу і зменшується зліва направо (в елементах головних груп) Електронегативність — зменшується зверху до низу і збільшується зліва направо (виняток Інертні гази)
У періодах зі зростанням протонного числа радіус атомів зменшується. У головних підгрупах зі зростанням протонного числа радіус атомів зростає (рис. 1).
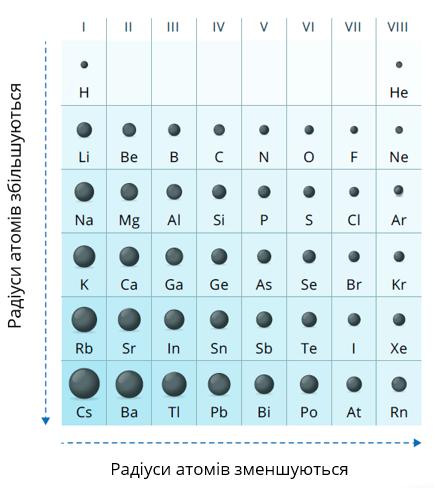

Атомний радіус вимірюється в пікометрах або ангстремах. 1. Половина віддалі, на якій знаходяться сусідні атоми в структурі простої речовини.